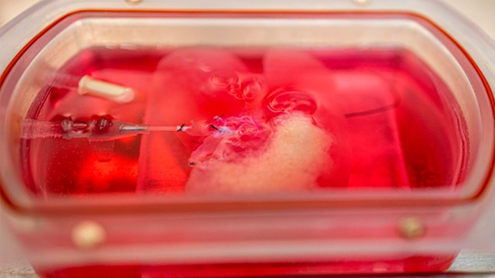
Fotografía del hígado de rata, despojada de células específicas de rata y resembrada con células hepáticas humanas. Crédito: UPMC.
Mini hígados humanos genéticamente modificados y cultivados en el laboratorio
07 de Agosto de 2019 | Historia original de la Escuela de Medicina de la Universidad de Pittsburgh
Los investigadores de la Escuela de Medicina de la Universidad de Pittsburgh fueron los primeros en cultivar hígados humanos en miniatura modificados genéticamente en el laboratorio, para emular la progresión de una enfermedad hepática humana y probar terapias.
En un artículo de prueba de concepto, publicado en Cell Metabolism, los investigadores de Pitt narran cómo transformaron células humanas genéticamente diseñadas en tejido hepático 3D funcional, que imita la enfermedad del hígado graso no alcohólico (NAFLD) -una condición que implica acumulación de grasa en el hígado-, que puede conducir a cirrosis o incluso insuficiencia hepática. Con la escalada de las tasas de obesidad en Estados Unidos, NAFLD se está convirtiendo rápidamente en la principal causa de enfermedad hepática crónica.
“Por primera vez pudimos crear mini hígados humanos modificados genéticamente con una enfermedad, usando células madre en el laboratorio", dijo el autor principal Alejandro Soto-Gutiérrez, M.D., PhD, profesor asociado de patología en la Escuela de Medicina de Pitt y miembro de la facultad del Instituto McGowan de Medicina Regenerativa y el Centro de Investigación del Hígado de Pittsburgh.
Esto es importante no sólo para entender qué causa la enfermedad y cómo progresa, sino también para probar terapias. Es común que los medicamentos fracasen en los ensayos clínicos, a pesar de los resultados prometedores en ratones.
Por ejemplo, el fármaco Resveratrol, que actúa sobre las proteínas SIRT11 comúnmente asociadas con NAFLD, fue eficaz en modelos murinos, pero fracasó en ensayos clínicos en humanos.
“Los ratones no son humanos”, dijo Soto-Gutiérrez. “Nacemos con ciertas mutaciones y polimorfismos, que nos predisponen a ciertas enfermedades, pero no se pueden estudiar polimorfismos en ratones, por lo que lograr un mini hígado humano personalizado es ventajoso.”
En primer lugar, los investigadores diseñaron genéticamente células normales de la piel humana que expresan un interruptor activable químicamente que podría amortiguar el gen SIRT1. Luego, reprogramaron las células a su estado de células madre y las convirtieron en células hepáticas. Después de eso, sembraron las células hepáticas humanas genéticamente diseñadas en hígados de rata despojados de sus propias células, donde proliferaron formando mini hígados 3D funcionales, con vasos sanguíneos y otras características estructurales de un órgano normal.
Esa estructura es parte de lo que distingue a los mini hígados de los cultivos 'organoides' (pequeñas esferas de células que se auto ensamblan para replicar la función orgánica simplificada), aunque los mini hígados carecieron de las distintas zonas de funciones metabólicas que poseen los hígados normales.
Una vez que los mini hígados maduraron, los investigadores activaron el interruptor genético para suprimir el gen SIRT1, y los mini hígados bioingenierizados comenzaron a imitar la disfunción metabólica observada en los tejidos de pacientes con enfermedad del hígado graso.
Pero al igual que los ensayos clínicos, Resveratrol tampoco fue eficaz en los hígados cultivados en laboratorio.
La clave, explicó Soto-Gutiérrez, es que el resveratrol aumenta la actividad de las proteínas SIRT1, no los genes SIRT1. Si se suprime la expresión génica SIRT1, como en los hígados bioingenierizados, y tal vez también en pacientes con NAFLD, no hay proteína sobre la que actuar, por lo que el medicamento no funcionará. Se está apuntando al paso equivocado.
“Esa es una visión que sólo podría provenir del estudio del tejido humano funcional”, dijo Soto-Gutiérrez.
Los mini hígados de ingeniería genética, cultivados en laboratorio proporcionan un banco de pruebas listo y confiable para medicamentos en todas las etapas de progresión de la enfermedad.
“Estos mini hígados aún no son adecuados para aplicaciones clínicas como el trasplante, pero imagino que en el futuro podemos lograr construir hígados humanos en los que se pueda programar la función uno desee, o incluso mejorar una función”, agregó Soto-Gutiérrez.
1 SIRT1 o Sirtuina 1, también conocida como “Sirtuína-1 desacetilasa dependiente de NAD”, es una proteína codificada por el gen "SIRT1".
SIRT1 significa "sirtuína (homólogo 2 de regulación de información de tipo unión silente) (S. cerevisiae), en referencia al hecho de que su homólogo (equivalente biológico a través de especies) en levadura (S. cerevisiae) es la Sir2. SIRT1 es una enzima desacetilasa que contribuye a la regulación celular (respuesta a estresores, longevidad y otros factores homeostáticos).
Este artículo ha sido republicado a partir de los siguientes materiales y editado para adecuar su longitud y contenido. Para obtener más información, ver la fuente citada.
Referencia: Collin de l’Hortet et al. 2019. Generation of Human Fatty Livers Using Custom-Engineered Induced Pluripotent Stem Cells with Modifiable SIRT1 Metabolism. Cell Metabolism. DOI: https://doi.org/10.1016/j.cmet.2019.06.017.
