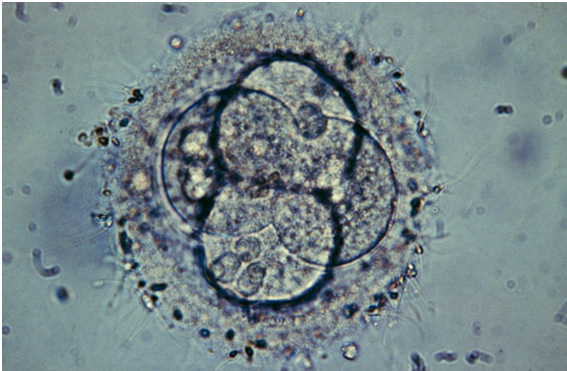
Foto: Los embriones humanos podrían editarse para corregir genes que causan enfermedades genéticas. Pero la ciencia es controversial. Crédito: Andy Walker, Midland Fertility Services/Science Photo Library
Más allá de los bebés CRISPR: cómo avanza la edición del genoma humano después del escándalo
Nature, 2 marzo 2023
Los investigadores discutirán los avances en las tecnologías de edición del genoma, y la ética de implementarlas, en una importante cumbre internacional.
Heidi Ledford
Cuando los investigadores se reúnan en Londres la próxima semana para la Tercera Cumbre Internacional sobre Edición del Genoma Humano, discutirán los últimos avances en el despliegue de técnicas como CRISPR-Cas9 para tratar enfermedades genéticas, y mirarán hacia la posible aprobación de la primera terapia basada en la edición del genoma a finales de este año.
A pesar de ese futuro tentador, será imposible sacudirse la sombra proyectada por la cumbre anterior, en 2018. Esa reunión se convocó solo un día después de que el biofísico He Jiankui anunciara que había editado los genomas de tres embriones que se convirtieron en bebés vivos. El truco finalmente le valió tres años de prisión por violar las leyes chinas sobre experimentos médicos.
Casi cinco años después, los investigadores le dicen a Nature que no esperan una revelación similar en la cumbre de este año, aunque solo sea porque la experiencia de He disuadirá a los investigadores deshonestos de hacer públicos los controvertidos experimentos de edición del genoma. Pero eso no significa que tales experimentos no estén ocurriendo: “No me sorprendería si hubiera otros niños creados con CRISPR-Cas9 en los años posteriores a 2018”, sostiene Eben Kirksey, antropólogo médico de la Universidad de Oxford, Reino Unido.
Desde entonces, los aspectos tecnológicos del uso de la edición del genoma para alterar embriones humanos con fines reproductivos no han cambiado fundamentalmente, dice Robin Lovell-Badge, bióloga reproductiva del Instituto Francis Crick de Londres que preside la cumbre. “Todavía es una técnica insegura”, dice, haciéndose eco de un consenso científico generalizado de que la tecnología de edición del genoma no está lista para su uso en embriones humanos .
En los años transcurridos desde las revelaciones de He, los investigadores han descubierto más preocupaciones sobre el uso de CRISPR-Cas9 en embriones, incluido el hecho de que puede barajar grandes segmentos de cromosomas . Esto se suma a otros problemas potenciales con la técnica, incluida la posibilidad de causar cambios genéticos no deseados y de generar un feto con un mosaico de células editadas y no editadas.
Falta regulación
Desde un punto de vista regulatorio, muchos países, incluido Estados Unidos, aún no cuentan con mecanismos para garantizar que no se implanten embriones editados, sostiene Kirksey. En febrero, China publicó nuevas directrices sobre conducta ética en la investigación biológica y médica. Estos abordan la necesidad de informar a los participantes del estudio sobre los riesgos potenciales y brindan una descripción detallada de cómo deben funcionar las juntas de revisión ética, dice Joy Zhang, socióloga de la Universidad de Kent en Canterbury, Reino Unido. Pero todavía confían en el modelo convencional de investigación médica basado en hospitales, institutos de investigación y universidades, dice ella. “Ignoran el hecho de que, en realidad, cada vez más, las empresas privadas o incluso los individuos pueden iniciar un proyecto de investigación que podría ser bastante dañino y de vanguardia”, dice. “Necesitamos repensar cómo gobernamos”.
Eso incluye reconocer que las restricciones sobre cómo se pueden gastar los fondos de investigación del gobierno podrían tener una influencia decreciente en el comportamiento de los investigadores, dice Zhang. Desde que salió de prisión, ha estado cortejando a inversores privados para que respalden un nuevo proyecto de terapia génica para la distrofia muscular de Duchenne. “La pregunta más importante que planteó He Jiankui no fue tanto la creación de bebés de diseño per se, sino el hecho de que hay un número creciente de prácticas científicas que están fuera de las instituciones científicas convencionales”, dice Zhang. “¿Cómo los rastreamos?”
Además, las regulaciones nacionales no toman en cuenta el posible alcance internacional de la edición hereditaria del genoma, dice María de Jesús Medina Arellano, abogada de derechos humanos de la Universidad Nacional Autónoma de México en la Ciudad de México. “No es que no haya leyes. Hay muchas leyes”, dice. “Necesitamos cambiar el enfoque de la aplicación. Esto debería ser considerado una jurisdicción internacional”.
Preocupaciones de asequibilidad
Los investigadores que desarrollan técnicas para editar genomas en células no reproductivas o somáticas también se enfrentan a un dilema inminente: ¿cómo garantizar que las terapias sean ampliamente accesibles? En 2018, hubo muy pocos ensayos de terapias de edición del genoma somático; ahora hay más de 100, dice Lovell-Badge. “Cada semana, parece que hay uno nuevo”.
Pero los precios de las terapias génicas existentes se están disparando, lo que hace que los investigadores se preocupen de que las terapias de edición del genoma sean igualmente inasequibles para gran parte del mundo. En noviembre, la Administración de Drogas y Alimentos de EE. UU. aprobó una terapia génica para tratar la hemofilia que tiene un precio de 3,5 millones de dólares estadounidenses por tratamiento. “Hay mucha esperanza, pero la esperanza tiene que equilibrarse un poco con la forma en que van las cosas”, dice Lovell-Badge.

He Jiankui dice que ahora está trabajando en una terapia génica para la distrofia muscular de Duchenne.
Varias sesiones de la reunión analizarán formas de garantizar el acceso en países de ingresos bajos y medianos, un tema de especial preocupación este año, ya que los reguladores de los Estados Unidos, el Reino Unido y la Unión Europea evalúan una solicitud de Vertex Pharmaceuticals en Boston. Massachusetts y CRISPR Therapeutics en Zug, Suiza, para aprobar una terapia CRISPR-Cas9 para la enfermedad de células falciformes, una condición genética que afecta principalmente a personas de ascendencia africana, india o del Medio Oriente. El tratamiento podría convertirse en la primera terapia de edición del genoma aprobada, pero los investigadores están observando con ansiedad para ver cuánto costará.
Durante el último año y medio, el cardiólogo Kiran Musunuru de la Universidad de Pensilvania en Filadelfia y sus colegas han estado desarrollando una terapia de edición del genoma para la enfermedad genética fenilcetonuria. El equipo está aprovechando variaciones del sistema CRISPR-Cas9 original que, a diferencia de CRISPR-Cas9, no implican la creación de roturas de doble cadena en el ADN. Se espera que estas técnicas, llamadas edición básica y edición principal, puedan producir terapias de edición del genoma más seguras. Pero Musunuru dice que es importante abordar la cuestión de la asequibilidad en las primeras etapas del desarrollo. “Veo un enorme potencial para las desigualdades”, sostiene.
Las tecnologías de edición del genoma también deben adaptarse a secuencias de ADN específicas. La relativa escasez de información sobre tales secuencias de personas de ascendencia no europea podría dejar regiones del mundo sin acceso a terapias de edición del genoma que funcionen para ellas.
Un desarrollo que podría facilitar el acceso en países de ingresos bajos y medianos es el esfuerzo por expandir la capacidad de fabricación de vacunas en el sur global . Algunas vacunas de ARNm contra la COVID-19 se basan en una nanopartícula lipídica para proteger la hebra de ARNm y ayudarla a penetrar las membranas celulares. Es posible que las terapias de edición del genoma, que también usan fragmentos de ARN, involucren sistemas de entrega similares, dice Musunuru, por lo que podrían usar la misma tecnología fundamental. “Si no hubiera sido por la pandemia, no estaríamos donde estamos”, dice. “Si me hubieran preguntado hace cinco años si podíamos hacer las cosas que podemos hacer ahora, habría dicho: “que eso es increíble, pero no'”.
Referencia: doi: https://doi.org/10.1038/d41586-023-00625-w
